摘要:乐德奇拜单抗 III 期研究数据公布
很多特应性皮炎(AD)患者都有类似的经历:
白天还算稳定,一到夜里却瘙痒加重,反复抓挠;
皮疹刚有所缓解,没过多久又卷土重来。
……
这种「好一点又复发」的循环,几乎贯穿了疾病的整个过程。也正因如此,AD不仅仅是「皮肤问题」,更在长期影响着患者的睡眠、情绪与生活质量。
在临床治疗中,一个越来越被重视的难题是:不少方案可以在短期内缓解症状,但在皮损深度清除与长期稳定控制方面,仍存在一定局限。如何在保证安全性的前提下,实现更持久、更稳定的疾病管理,仍是中重度AD治疗亟待突破的关键问题。
随着精准医学时代的到来,生物靶向药物的崛起为破局带来了曙光。2026年3月28日,第84届美国皮肤科学会年会(AAD)在美国科罗拉多州丹佛市盛大召开。作为全球皮肤病学领域的顶级学术盛会,本次大会见证了里程碑式的一刻:北京大学人民医院皮肤科主任周城教授在大会现场对创新抗体药物——乐德奇拜单抗的Ⅲ期临床研究结果进行口头报告。结果显示,跟安慰剂组对比下,乐德奇拜单抗的研究结果表现出安全、有效、整体耐受性良好的结果。该研究由北京大学人民医院张建中教授和周城教授联合牵头担任主要研究者,共有 59 家医院参与。这一突破性成果作为最新突破性摘要(Late-Breaking Research)在现场公布,无疑为中重度AD的长期管理与深度治愈开启了全新的篇章。(乐德奇拜单抗是先声药业与康乃德生物医药合作的创新抗体药物,此次公布的是其在成人及青少年中重度特应性皮炎患者中开展的Ⅲ期临床研究数据)

图1 周城教授在 AAD 大会演讲
从源头入手:靶向IL-4通路的精准治疗新思路
如果说特应性皮炎(AD)是一场发生在皮肤上的「风暴」,那么2型炎症通路就是这场风暴的关键源头,而白细胞介素-4(IL-4)不仅启动了过敏反应,更维持了炎症的持续存在[1]。
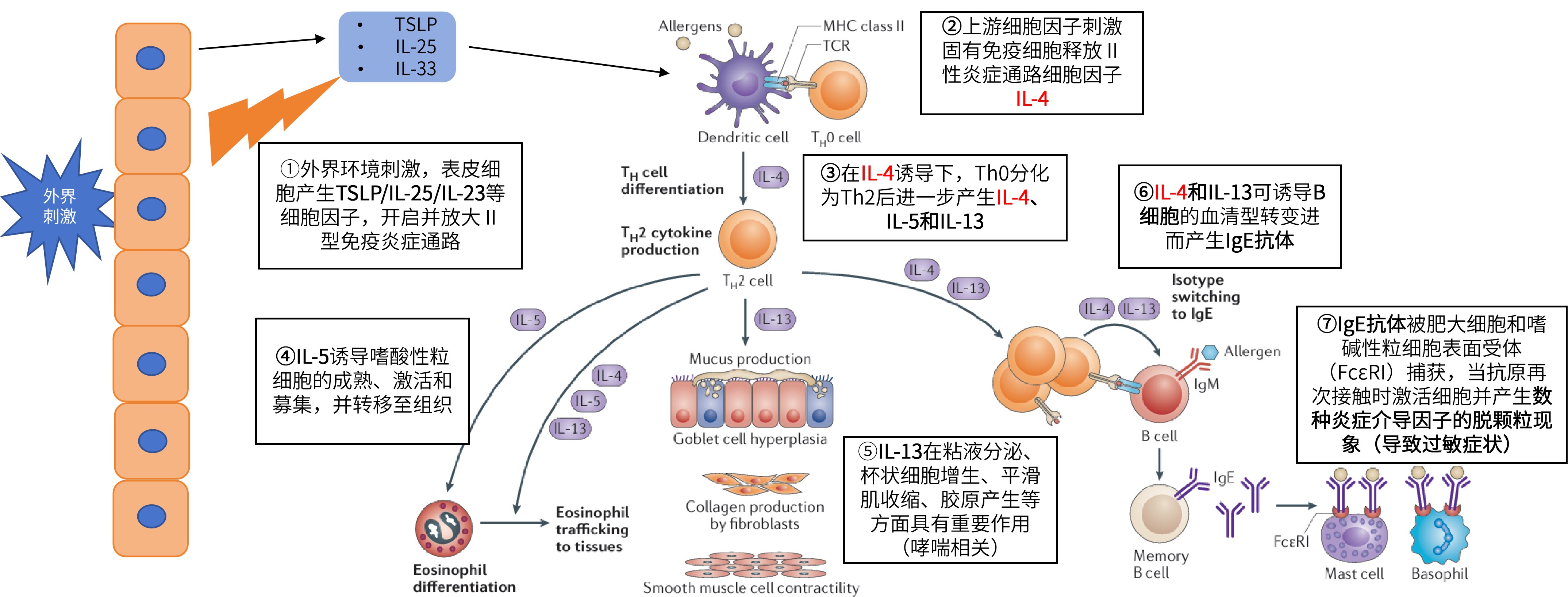
图2 IL-4在Ⅱ型炎症通路中发挥重要作用[1]
乐德奇拜单抗,正是基于这样的机制应运而生的新一代生物制剂。作为一种靶向IL-4受体α亚基(IL-4Rα)的全人源单克隆抗体,它如同一名精准的「狙击手」,直击致病源头,为中重度AD的系统治疗开辟了全新的航道。
在前期研究中,该药物已显示出良好的疗效和安全性基础[2-4],而此次公布的Ⅲ期临床研究,则进一步验证了其在实际治疗中的效果与安全表现。RADIANT-AD是一项严谨的随机、双盲、安慰剂对照Ⅲ期临床研究,旨在全面评估乐德奇拜单抗用于AD治疗的疗效与安全性。
|
研究纳入259例12岁以上中重度AD患者,随机分为乐德奇拜单抗组(n=128)和安慰剂组(n=131):
²乐德奇拜单抗组:首剂600mg,随后300 mg每2周一次(Q2W)维持治疗,全程持续用药(52周)
²安慰剂组:前16周给予安慰剂,16周后切换为乐德奇拜单抗300mg 每2周一次(Q2W),持续治疗36周
主要终点为第16周时,IGA评分达0/1分且较基线降低≥2分的患者比例,以及EASI评分较基线改善≥75%(EASI-75)的患者比例。
|
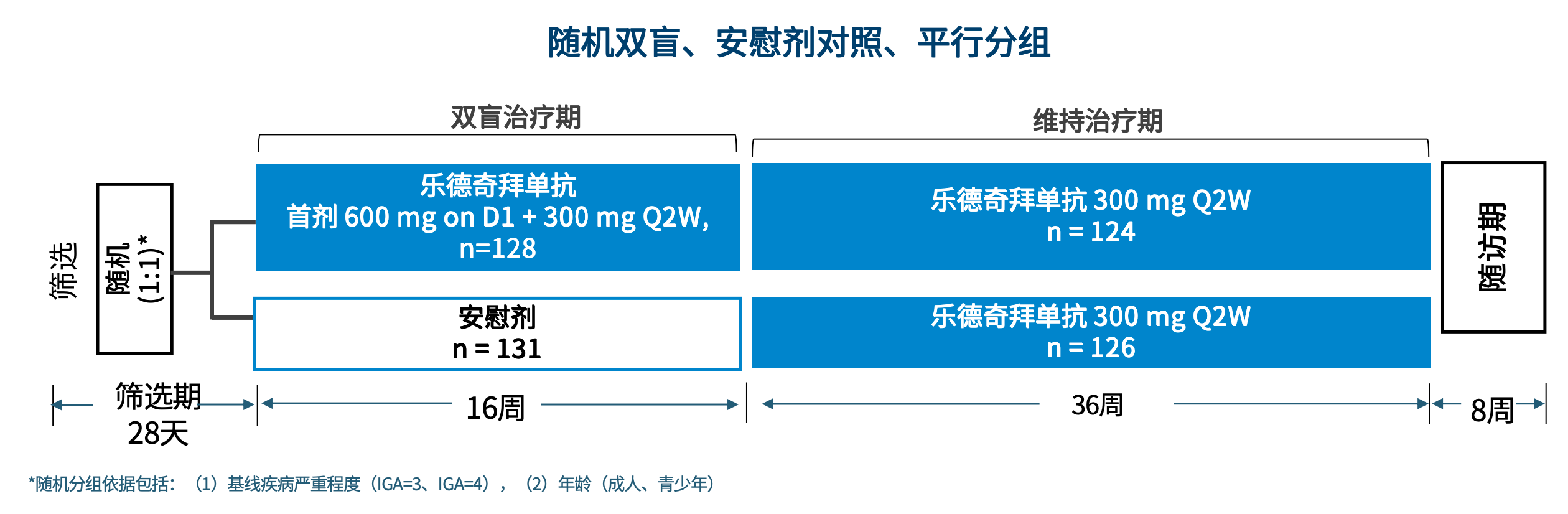
图3 RADIANT-AD研究设计
长期疗效、深度清除皮损与安全耐受的三维验证
快速起效、持久护航,高应答率铸就长期稳态
RADIANT-AD研究中,乐德奇拜单抗展现出了令人瞩目的「速效」与「长效」双重优势。根据本次AAD大会公布的数据,在早期评估时间点已观察到其与安慰剂组的疗效差异,并在第16周(诱导期终点)进一步得到确认。第16周时,乐德奇拜单抗组的EASI-75应答率(74.2%)显著高于安慰剂组(34.4%)(p < 0.0001),提示其在早期即可实现较为明确的疗效获益。
随着治疗延续至第52周,乐德奇拜单抗组EASI-75应答率进一步攀升至96.6%,显示出持续增强的疗效及良好的长期疾病控制能力。同时,在由安慰剂转换为乐德奇拜单抗治疗的患者中,应答率亦快速提升,并在第52周达到95.9%,提示该治疗在不同治疗阶段均可带来稳定的疗效获益。
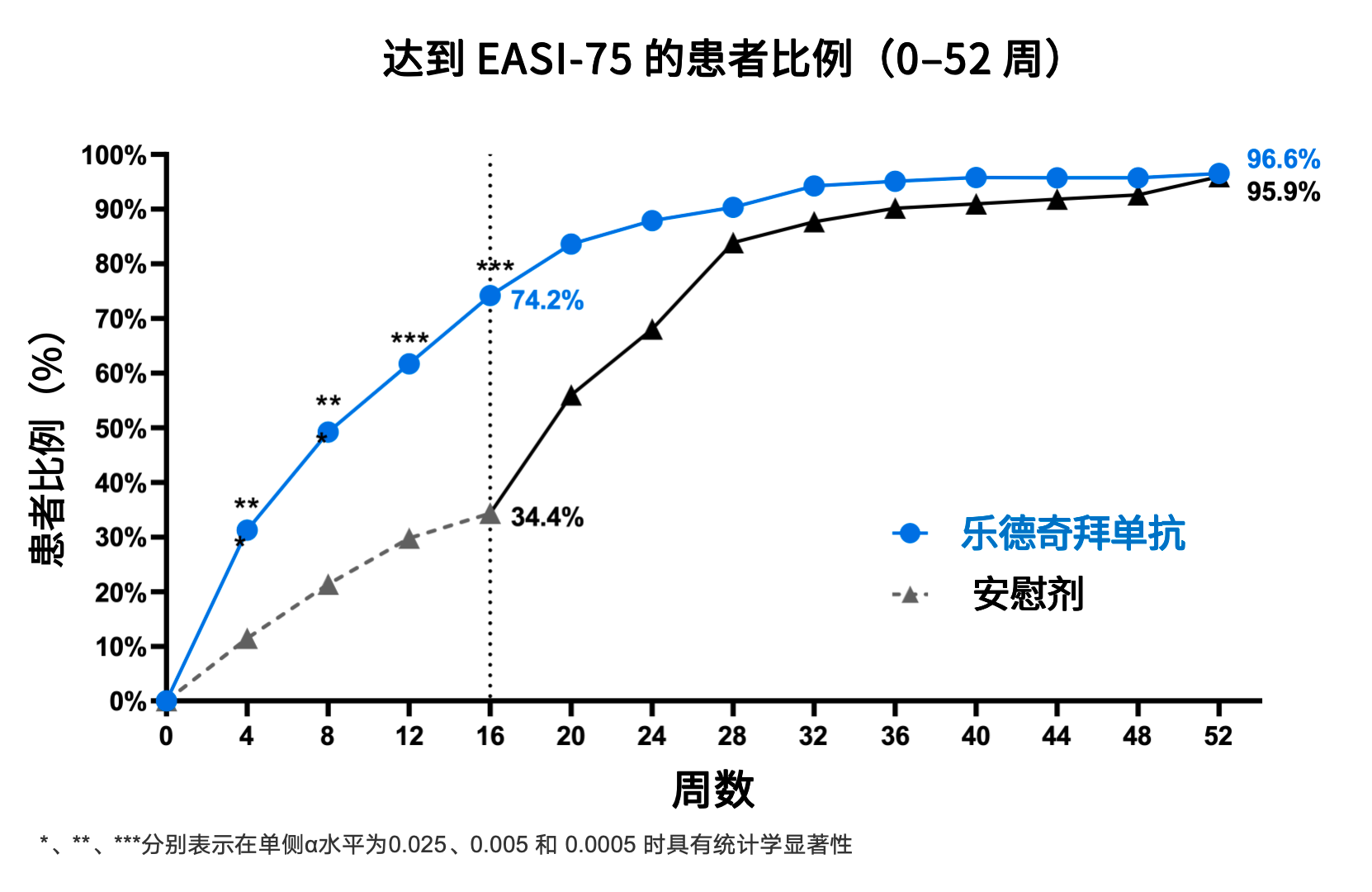
图4 乐德奇拜单抗与安慰剂组第16周和52周EASI-75应答率
深度缓解,重塑皮肤屏障,迈向「完全清除」的持续获益
AD治疗的目标不仅是改善症状,更在于清除皮损。RADIANT-AD研究显示,乐德奇拜单抗在推动疾病深度缓解方面表现卓越。
在第16周时,已有47.7%的患者达到了皮损完全清除或几乎清除(IGA 0/1)的理想状态,显著高于安慰剂组的17.6%(p < 0.0001)。继续治疗至第52周,乐德奇拜单抗组的IGA 0/1应答率接近90%。这意味着对AD患者而言,「皮损完全清除」或许已不再是难以企及的目标。同时,即便是后期转换治疗的患者,其IGA 0/1应答率同样显著提升至75.6%。
这些数据进一步支持了Ⅲ期临床研究中乐德奇拜单抗在皮损清除方面的疗效表现,并提示长期规范治疗可能为患者带来持续累积的临床获益。
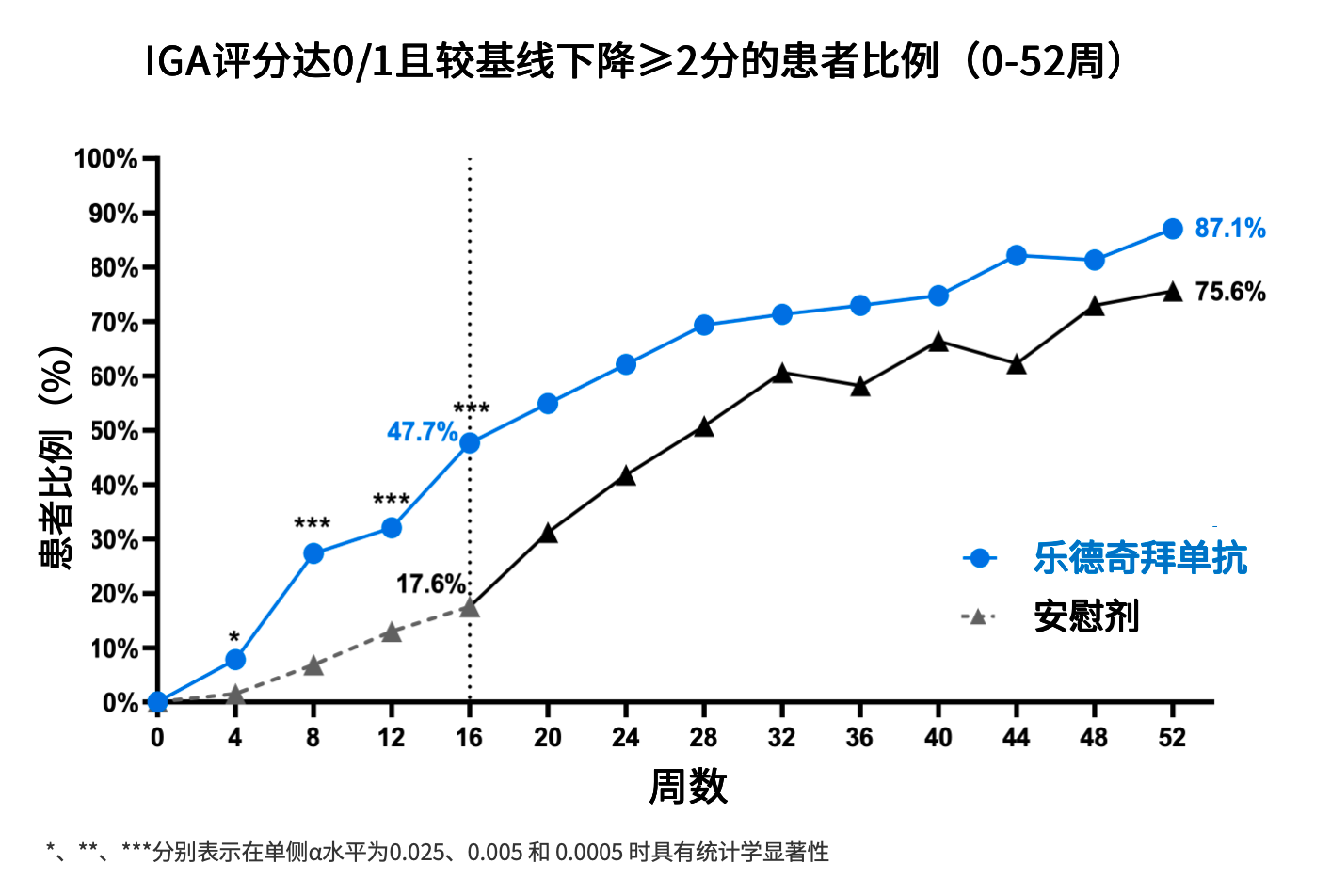
图5 乐德奇拜单抗与安慰剂组第16周和52周IGA 0/1应答率
安全性、耐受性良好,兼顾疗效与低用药负担
安全性方面,在前16周诱导期内,研究未观察到任何与研究药物相关的严重不良事件(SAE)或≥3级不良事件(AE),安全性表现良好。常见的不良事件如注射部位反应及结膜炎的发生率极低,分别为1.6%和3.9%,且这些数值与安慰剂组相当,表明药物并未额外增加患者的健康风险。
从分子机制到临床结局的综合证据
• 高亲和力
乐德奇拜单抗对IL-4Rα展现出较高的结合亲和力,其解离常数(KD)低至20.7 pM,相比之下,度普利尤单抗的KD值为45.8 pM。更低的KD值意味着药物更倾向于与靶点结合,即使在低浓度下也能有效阻断炎症通路的信号传导[5]。
• 种属特异性强
乐德奇拜单抗仅与人源IL-4Rα发生结合,而不与猴、鼠、狗、大鼠或兔等非人灵长类或哺乳动物的受体产生交叉反应,这种精准的「识别能力」奠定了药物在人体内作用专一性的基础[5]。
• 抑制炎症基因表达
在细胞层面,乐德奇拜单抗可有效抑制由IL-4介导的下游炎症基因表达,在基因水平上深入「关闭」了驱动特应性皮炎持续恶化的开关[5]。
• 深度清除与持久应答
Ⅲ期临床研究显示,乐德奇拜单抗不仅能有效改善症状,更具备强大的皮损深度清除能力。随着治疗时间的延长,患者的应答率持续攀升,展现出长期稳定性的特性。
• 转换治疗的迅速获益
尤为值得一提的是,安慰剂组患者后期转换为乐德奇拜单抗治疗,同样取得了令人满意的疗效,进一步明确了药物长期、稳定的临床获益。
• 可控的不良事件
在治疗前16周内,未观察到与药物相关的严重不良事件(SAE),且SAE发生率与安慰剂组相当。在52周随访期间,,未见新的安全性信号,提示其具备良好的长期安全性特征。此外,常见不良事件如结膜炎发生率较低(6.3%),整体安全性表现可控。
在上述研究结果的基础上,有必要关注其背后的分子设计与开发过程。乐德奇拜单抗历经十余年研发,已在全球开展12项临床研究(其中10项已完成),包括剂量递增研究、药代/药效学研究及随机对照研究等,累计超过1500例受试者暴露,其中中重度特应性皮炎相关研究5项,逐步积累了系统性证据,为其机制相关特征提供了支持。
总结
长期以来,AD患者深陷「诱导期应答不足」与「皮损深度清除难」的临床困境,中重度患者亟须兼具高效与安全的创新疗法。
乐德奇拜单抗作为新一代IL-4Rα靶向生物制剂,在临床前研究中展现出高靶点亲和力、严格物种特异性与炎症抑制能力的核心优势,为其在AD等2型炎症疾病中的优异临床疗效奠定了坚实的机制基础。
关键性Ⅲ期临床研究(RADIANT-AD)进一步验证了乐德奇拜单抗在12岁及以上中重度AD患者中的疗效与安全性。数据显示,治疗第16周,乐德奇拜单抗组在皮损深度清除(EASI-75)与疾病控制(IGA 0/1)指标上均显著优于安慰剂组;至第52周,持续治疗组应答率进一步攀升至高水准,且安慰剂转换组在启用药物后亦迅速获益,佐证了其起效快、疗效深且持久的特点。安全性方面,乐德奇拜单抗治疗16周未发生药物相关严重不良事件,整体耐受性良好,并在此基础上使部分患者实现皮损接近完全清除成为可能。
✩ 本文仅供医疗卫生等专业人士参考
参考文献
[1] Gandhi NA, Bennett BL, Graham NM, Pirozzi G, Stahl N, Yancopoulos GD. Targeting key proximal drivers of type 2 inflammation in disease. Nat Rev Drug Discov. 2016;15(1):35-50.
[2] Wang J, White J, Sansone KJ, et al. Rademikibart (CBP-201), a next-generation monoclonal antibody targeting human IL-4Rα: Two phase I randomized trials, in healthy individuals and patients with atopic dermatitis. Clin Transl Sci. 2023;16(12):2614-2627.
[3] Silverberg JI, Strober B, Feinstein B, et al. Efficacy and safety of rademikibart (CBP-201), a next-generation mAb targeting IL-4Rα, in adults with moderate to severe atopic dermatitis: A phase 2 randomized trial (CBP-201-WW001). J Allergy Clin Immunol. 2024;153(4):1040-1049.e12.
[4] Zhang J, Silverberg JI, Guo J, et al. Rademikibart monotherapy for moderate-to-severe atopic dermatitis in a 1-year, randomized phase II trial (SEASIDE CHINA): initial 2-week dosing, followed by 2-week or 4-week dosing. Br J Dermatol. 2026;194(1):47-58.
[5] Zhang, L, Ding, Y, Wang, Q, et al. Preclinical immunological characterization of rademikibart (CBP-201), a next-generation human monoclonal antibody targeting IL-4Rα, for the treatment of Th2 inflammatory diseases. Sci Rep. 2023; 13 (1): 12411.
